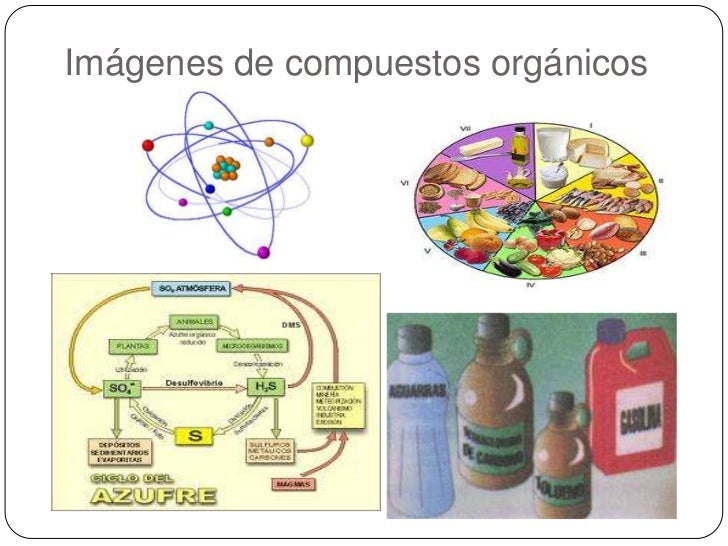
Los ácidos resultan de la combinación de
óxidos no metales (anhídridos) con
el agua, a estos ácidos se le denomina oxácidos o ácidos ternarios, son
aquellos que están formados por 3 elementos (hidrógeno, no metal y oxígeno)
Los ácidos también resultan de la combinación
del hidrógeno con los elementos halógenos (cloro, yodo, bromo y flúor ) dando
como resultado hidrácidos o ácidos binarios, son aquellos que están formados por
dos elementos (metal y no metal), y por lo tanto no tiene oxígeno en su
composición . Ambos se nombran antecediendo la palabra ácido seguida de la
terminación oso o hipo-oso si es un oxácido, y el no metal terminado en hídrico
en el caso de los hidrácidos
Ejemplo:
Oxácidos
Co2 +H2O --- H2CO3 Ácido carbónico
Hidrácidos
H2 + C L2 ----- 2HCL Ácido clorhídrico